FDA News Release
La FDA alerta a los consumidores sobre el retiro voluntario del mercado en todo el país de EpiPen y EpiPen Jr
- For Immediate Release:
La Administración de Alimentos y Medicamentos de los EE. UU. (FDA, por sus siglas en inglés) alerta a los consumidores sobre la retiro voluntario del mercado que realizó Meridian Medical Technologies de 13 lotes de autoinyectores EpiPen y EpiPen Jr (inyección de epinefrina) utilizados para el tratamiento de emergencia de reacciones alérgicas graves. Este retiro se debe a la posibilidad de que estos aparatos puedan contener una pieza defectuosa que podría hacer que estos no se activen. El producto retirado fue fabricado por Meridian Medical Technologies y distribuido por Mylan Specialty.
Si bien el número de fallos denunciados es pequeño, los productos EpiPen que posiblemente contengan una pieza defectuosa están siendo retirados debido a la posibilidad que presente un riesgo potencialmente mortal si una reacción alérgica grave no es tratada. Los consumidores deben conservar y usar su EpiPen actual si lo necesitan hasta recibir uno nuevo. Deben comunicarse con Mylan al 800-796-9526 o escribir a customer.service@mylan.com si tienen alguna pregunta.
Como se indica en la etiqueta del producto, los consumidores siempre deben buscar ayuda médica de emergencia cuanto antes después de usar sus EpiPen, en particular, si el aparato no se activó.
En este momento, los 13 lotes identificados —distribuidos entre el 17 de diciembre de 2015 y el 1.° de julio de 2016— son los únicos lotes de EpiPen afectados por la retirada de los EE. UU. Los consumidores que tengan EpiPen de lotes que no estén incluidos en esta retirada no tienen que cambiar su EpiPen antes de la fecha de vencimiento.
| Producto/Dosis | Número de NDC | Número de Lote | Fecha de Expiración |
|---|---|---|---|
| EpiPen Jr Auto-Injector, 0.15 mg | 49502-501-02 | 5GN767 | Abril 2017 |
| EpiPen Jr Auto-Injector, 0.15 mg | 49502-501-02 | 5GN773 | Abril 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 5GM631 | Abril 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 5GM640 | Mayo 2017 |
| EpiPen Jr Auto-Injector, 0.15 mg | 49502-501-02 | 6GN215 | Septiembre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM082 | Septiembre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM072 | Septiembre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM081 | Septiembre 2017 |
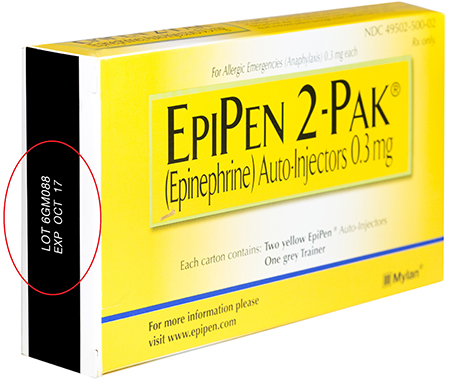
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM088 | Octubre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM199 | Octubre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM091 | Octubre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM198 | Octubre 2017 |
| EpiPen Auto-Injector, 0.3 mg | 49502-500-02 | 6GM087 | Octubre 2017 |
La FDA solicita a los profesionales sanitarios y a los consumidores denunciar cualquier reacción adversa o mal funcionamiento de los aparatos al programa MedWatch de la FDA:
- Llenando y enviando el reporte en línea a www.fda.gov/medwatch/report.htm, o
- descargando y completando el formulario y luego enviándolo por fax al 800-FDA-0178.
La FDA, una dependencia del Departamento de Salud y Servicios Sociales de los Estados Unidos, protege la salud pública asegurando la protección, eficacia y seguridad de los medicamentos tanto veterinarios como para los seres humanos, las vacunas y otros productos biológicos destinados al uso en seres humanos, así como de los dispositivos médicos. La dependencia también es responsable de la protección y seguridad de nuestro suministro nacional de alimentos, los cosméticos, los suplementos dietéticos, los productos que emiten radiación electrónica, así como de la regulación de los productos de tabaco.
###
Inquiries
- Media:
- Gloria Sánchez-Contreras
- 301-796-7686
- Consumer:
- 888-INFO-FDA